
2019年10月22日,厦门大学神经科学研究所张杰教授课题组在国际神经科学顶级期刊《Nature Neuroscience》(IF=19.912)上合作发表题为“Age-related hyperinsulinemia leads to insulin resistance in neurons and cell-cycle-induced senescence”的研究论文,首次揭示了神经系统的胰岛素抵抗会通过诱导细胞周期重启导致神经元衰老的现象和机制,为T2D和AD的诊治提供了新的理论基础和靶点。
二型糖尿病(T2D)和阿尔茨海默病(AD)都是非常严重的影响人类健康的公共健康问题。全世界有超过四亿的糖尿病患者和超过一亿的AD患者,给个人、家庭和社会带来沉重的负担。T2D和AD的发病率都随着衰老而逐渐增加,并且越来越多的流行性病学研究证实二型糖尿病患者往往伴随着学习认知功能的障碍,并是阿尔茨海默病发病的一个重要诱因,然而其中具体的关联机制还不清楚。
导致二型糖尿病的一个关键诱因是高糖诱导产生的机体对胰岛素的抵抗(Insulin Resistance-IR), 进而产生高胰岛素血症(Hyperinsulinemia),对机体产生很多损伤,其中也包括大脑。外周高胰岛素会通过主动运输的方式进入大脑;短期的胰岛素暴露对神经元的代谢具有支持作用,但长期的脑部高胰岛素也会导致大脑Hyperinsulinemia,并诱导神经元的胰岛素抵抗和增加AD的发生的风险。但脑部高胰岛素水平是如何诱导神经元损伤以及增加AD风险的机制还有待阐明。该研究发现外周的高胰岛血症会导致大脑中的胰岛素水平升高导致神经元的胰岛素抵抗,进而会降低葡萄糖代谢的关键酶己糖激酶2(Hexokinase 2),从而导致神经元中糖酵解紊乱。同时HK2会调控细胞周期蛋白激酶CDK5的激活蛋白P35的累计,并诱导糖原合成酶GSK3beta的异常激活,导致beta-catenin的累计,从而激活神经元的细胞周期。神经元细胞周期的激活会导致神经元的衰老,衰老神经元表现出神经突触功能紊乱等损伤特征。
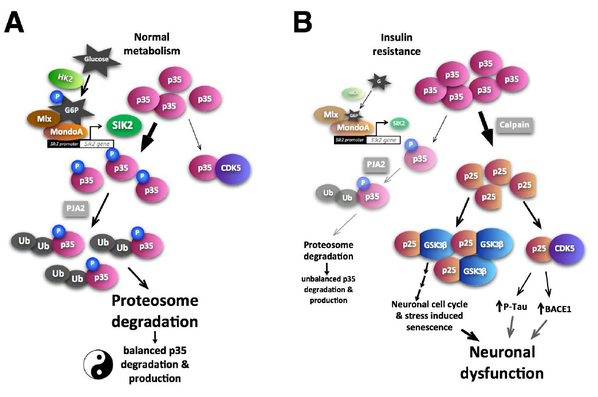
作为终端分化的细胞,神经元是否可以老化以及其老化的机制一直不清楚。该研究第一次提出是细胞周期重新激活而不是细胞周期抑制导致神经元衰老的新机制,对于理解包括阿尔茨海默病在内的神经退行性疾病具有重要的意义。
该项研究是由厦门大学张杰教授和香港中文大学的周熙文教授、美国匹兹堡大学的Karl Herrup教授合作完成的。周熙文、张杰和Karl Herrup为文章的共同通讯作者。张杰教授长期和周熙文、Karl Herrup合作在阿尔茨海默病和糖尿病的研究中取得了一系列的进展,文章先后发表在PNAS(2014), Biological Psychiatry (2019),Nature Neuroscience(2019)等。该研究得到了国家自然科学基金委“器官衰老与器官退行性变化的机制”重大研究计划和中央高校基本科研业务费(厦门大学校长基金)等的资助。

张杰教授课题组主要从事重大神经系统疾病(老年痴呆、抑郁症、自闭症、术后认知障碍)等的发病机制和药物开发研究。从神经炎症-细胞周期-细胞衰老-细胞死亡等多个角度系统研究和揭示了阿尔茨海默病、抑郁症等新的致病机制。作为通讯作者在国际知名期刊Nature Neuroscience, Neuron,Cell Reports, PNAS, Biological Psychiartry, The Journal of Neuroscience, Clinical Cancer Research,CDD, JBC, Chemistry,Chem. Biol. Drug Des.等杂志上发表多篇研究论文。目前承担包括自然科学基金委重点项目、优青项目、面上项目,国家重点研发计划、省市项目多项。
原文链接:https://www.nature.com/articles/s41593-019-0505-1

