阿尔茨海默病(AD)是全球老年人中最常见的与进行性认知衰退和记忆力丧失相关的痴呆类型。尽管AD的确切病因尚未完全明了,但越来越多的证据表明,β-淀粉样蛋白(Aβ)的过度产生及其伴随的神经炎症在AD的发病机制中起着关键作用。迄今为止,可用的AD治疗方法仅能部分缓解临床症状,因此迫切需要能够阻止或逆转Aβ诱导的神经炎症和认知障碍的治疗手段。小胶质细胞是中枢神经系统(CNS)中的主要先天免疫细胞,通过免疫监视维持正常脑功能,在神经炎症过程中起关键作用。在AD发病过程中,小胶质细胞因累积的Aβ而长期过度激活,并通过分泌促炎因子IL-1β、IL-6以及TNF-α等触发显著的神经毒性。这些炎症细胞因子不仅能促进Aβ的产生,还能反过来增强小胶质细胞对Aβ的反应,从而在Aβ诱导的发病机制和小胶质细胞介导的神经炎症之间形成恶性循环。然而,驱动AD中小胶质细胞炎症的关键因素尚未完全阐明。
2024年6月28日,厦门大学神经科学研究所赵颖俊教授团队与空军军医大学唐都医院神经内科张巍副教授团队合作在Alzheimer's & Dementia杂志上发表了题为 PKCδ serves as a potential biomarker and therapeutic target for microglia-mediated neuroinflammation in Alzheimer’s disease的研究论文。该团队发现蛋白激酶Cδ(PKCδ)在AD患者脑脊液(CSF)显著增加,并与炎症因子水平密切相关。进一步研究发现PKCδ在小胶质细胞中高表达,并调节小胶质细胞介导的炎症反应。总之,该研究揭示了PKCδ是AD中小胶质细胞介导的神经炎症的潜在生物标志物和治疗靶点。

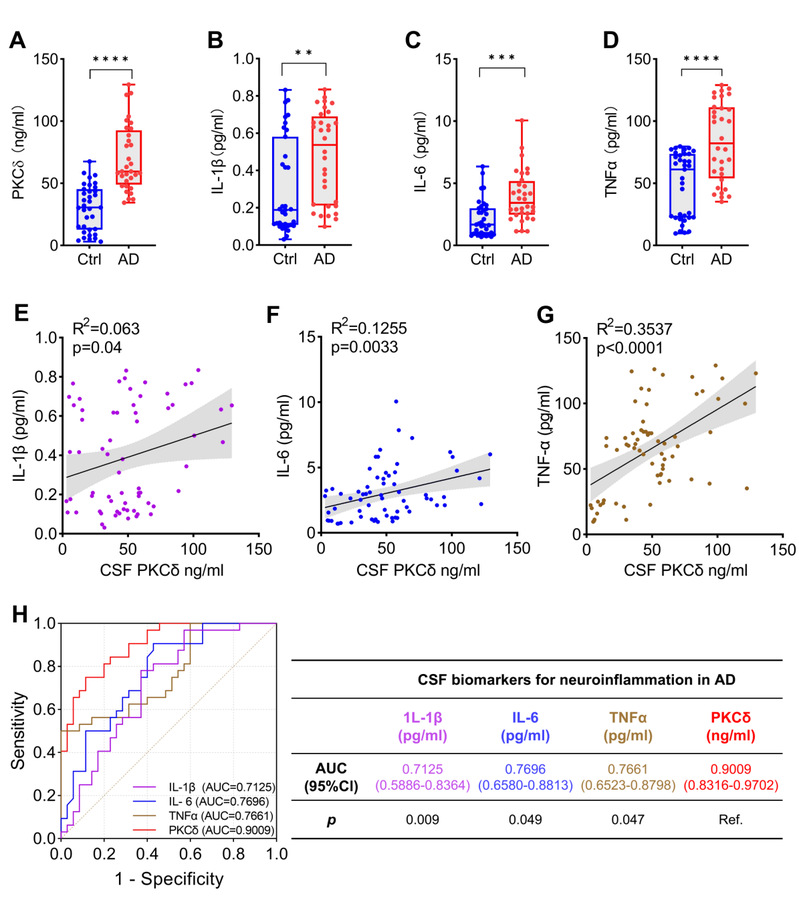
该团队首先通过ELISA来测定来自32名A+T+(N)痴呆患者(AD组)和35名A-T-(N)正常认知参与者(NC组)的CSF样品中PKCδ和与AD相关的炎性因子水平,结果显示,与正常对照组相比,AD患者CSF中PKCδ、IL-1β、IL-6和TNF-α的水平均显著升高。并且PKCδ水平与测试的细胞因子水平呈正相关。ROC分析显示,PKCδ的曲线下面积(AUC)显著大于TNF-α、IL-1β和IL-6,表明PKCδ在区分AD和非AD受试者方面优于经典炎症蛋白。为了验证以上结果,团队成员进一步对APPswe/PS1dE9小鼠的脑内PKCδ和与AD相关的炎性因子水平进行检测,结果显示PKCδ水平分别与IL-1β、IL-6和TNF-α水平呈正相关。这些结果表明PKCδ 可能是AD的神经炎症生物标志物,并参与AD相关的神经炎症。
接下来研究人员对CSF中 PKCδ 的来源进行了探索,结果发现在原代培养的小胶质细胞中PKCδ 的蛋白质水平最高,与此同时,在WT和APPswe/PS1dE9小鼠的大脑中也发现PKCδ 主要在IBA1+小胶质细胞中高表达。并且,研究人员对AD人脑数据集(GSE157827)的分析也表明PKCδ 在人脑的小胶质细胞中高度表达。随后研究者在原代小胶质细胞的培养基中也检测到PKCδ 的表达,并发现寡聚物Aβ1-42和LPS可以调节PKCδ的表达和分泌。基于以上结果,研究者推测CSF中的PKCδ主要来源于小胶质细胞。
随后,为了确定PKCδ是否可以调节小胶质细胞介导的炎症,研究人员通过慢病毒过表达PKCδ,研究发现PKCδ的过表达显著减弱了小胶质细胞吞噬作用,并导致IL-1β、IL-6和TNF-α的mRNA水平显著升高。接下来通过RNAseq分析探索其潜在的机制,研究人员证实PKCδ 能够调节小胶质细胞炎症反应和Aβ诱导的NF-κB信号传导的改变。
最后,为了探究PKCδ是否在体内介导AD相关的神经炎症,研究人员通过使用PKCδ抑制剂rottlerin治疗6月龄的APPswe/PS1dE9小鼠,发现rottlerin治疗显著降低了AD小鼠大脑中PKCδ的表达和IκBα/p65磷酸化,并减轻小胶质细胞相关的神经炎症,此外,Morris水迷宫测试结果还显示Rottlerin治疗显著改善了AD小鼠的空间学习和记忆功能。以上结果表明,NF-κB通路参与了AD小鼠PKCδ 介导的神经炎症。
综上,该研究揭示了PKCδ作为小胶质细胞介导的神经炎症的特异性生物标志物,并表明抑制PKCδ可能是针对AD中由Aβ诱导的神经炎症损害的一种可行治疗策略。这一发现为AD的治疗提供了新的潜在靶点,有望为缓解神经炎症带来的损伤开辟新的治疗途径。
空军军医大学唐都医院神经内科张巍副教授及厦门大学赵颖俊教授为本论文通讯作者,空军军医大学唐都医院神经内科杜婴、郝云凤、李川以及厦门大学神经科学研究所郭田田为共同第一作者。最后,研究团队特别感谢厦门大学神经科学研究所创始人许华曦教授在本研究初期提供的宝贵建议和悉心指导,深切缅怀许华曦教授。

